脳内のグリア細胞―神経細胞間コミュニケーションを解き明かす
空間的分子探索技術の創出
慶應義塾大学医学部生理学
特任助教
髙野哲也
近年、脳内においてグリア細胞の一つであるアストロサイトは神経細胞のシナプスとの間に繋ぎ目を形成し、神経回路の形成や脳機能を制御していることが分かってきました。このアストロサイトと神経細胞の接着部位は「三者間シナプス」(図A)とも呼ばれ、三者間シナプスの機能破綻は多くの精神・神経疾患の原因の一つとされています。しかしながら、これまでの生化学的・分子生物学的手法では生体内における三者間シナプスの構成分子群を同定できなかった為、アストロサイトによるシナプス形成や脳機能制御に関わる分子機構については不明な点が多く残されていました。
近年、近位依存性ビオチン標識(BioID)法が開発され、近傍に存在し相互作用する分子群を網羅的に解読できるようになってきました。この方法では、標的の近傍にある分子が予めビオチン標識されるために、膜可溶化などの影響を受けずに分子群を解析できるという利点があります。私たちは、このBioID法をさらに発展させて、特定の異種細胞間の接着に関与する分子群を明らかにする新たなプロテオミクス技術Split-TurboID法を開発しました。Split-TurboID法では、高活性型ビオチン化酵素TurboIDをN末端とC末端に分割し、それぞれに柔軟なリンカー配列と細胞膜挿入配列を付加した人工タンパク質を作製し、隣り合う細胞に別々に発現させます。それにより、細胞同士が近接する接着部位でのみTurboIDのビオチン化活性が再構成されるため、接着部位近傍に存在する分子群をビオチン標識することができます(図A)。私たちは このSplit-TurboID法を用いて、これまで同定することが困難とされていた三者間シナプスを構成する分子群を網羅的に同定しました 。 次に、今回同定した新規三者間シナプス制御分子としてNRCAMという細胞接着分子に着目し、詳細な機能解析を行いました。その結果、NRCAMは生体内においてアストロサイトで高発現し、シナプス近傍のアストロサイトの微細突起上に局在していることが分かりました。興味深いことに、NRCAMは抑制性シナプスの足場タンパク質gephyrinを集積させることで抑制性シナプスの形成と機能を制御していました(図B)。これらの結果から、アストロサイトはNRCAMを介して抑制性シナプスの形成と機能を制御することで、脳神経回路のはたらきを調節していることが明らかになりました。
Takano T*, Wallace JT, Baldwin KT, Purkey A, Uezu A, Courtland JL, Soderblom EJ, Shimogori T, Maness PF, Eroglu C*, Soderling SH*. Chemico-genetic discovery of astrocytic control of inhibition in vivo. Nature, 2020 (*Co-corresponding authors) doi:10.1038/s41586-020-2926-0 (2020).
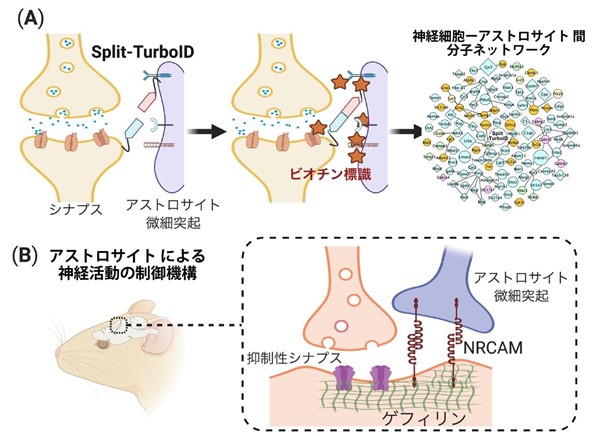
<図の説明>
(A) 生体内における異種細胞間相互作用分子の網羅的探索技術 Split-TurboID法の作動原理。 Split-TurboID法は、ビオチン化酵素TurboIDをN末端とC末端に2分割し、そこに柔軟なリンカー配列と細胞膜挿入配列を付加したものです。これらを、神経細胞とアストロサイトに発現させると、接着部位にてSplit-TurboIDの活性が再構成され、細胞接着分子や受容体、イオンチャネル分子など細胞間隙分子を網羅的にビオチン標識します。このSplit-TurboID法により多数の三者間シナプス構成分子を同定しました。
(B) アストロサイト特異的NRCAMによる抑制性シナプスの制御機構。アストロサイトのNRCAMはホモフィリック結合を介して、神経細胞の抑制性シナプス分子gephyrinを集積することで抑制性シナプスの形成と機能を制御していました。またアストロサイトのNRCAMを遺伝子欠損すると、アストロサイトの微細突起が複雑化し、抑制性シナプスの形成と機能に障害が見られました。
〈研究者の声〉
本研究は、Duke大学のScott Soderling研究室、Cagla Eroglu研究室、理化学研究所(CBS)の下郡智美先生らとの共同研究により行いました。本研究は分割型BioIDツールの設計・開発という全てが手探りの状態から始まったプロジェクトでした。本当に苦労も多かったのですが、振り返ってみますと、初めて三者間シナプスのプロテオーム データを見たときにSoderling博士やEroglu博士と一緒になって興奮して大喜びしたことが、つい先日のように鮮明に思い出されます。最後になりますが、多大なご助力を賜りました共同研究者の皆様に心より感謝申し上げます。今後は、これらの研究成果をさらに発展させて、脳機能の動作特性の探究や精神・神経疾患の研究にも貢献して行きたく思っております。
〈略歴〉
2013年3月 東京都立大学大学院理工学研究科、博士課程修了
2013年4月 名古屋大学大学院医学系研究科、神経情報薬理学講座、博士研究員
2015年4月 日本学術振興会―特別研究員PD
2018年4月 Department of Cell Biology, Duke University Medical School、博士研究員
2020年7月 慶應義塾大学医学部生理学、特任助教






