狂犬病ウイルス基礎情報
宮道和成 (理化学研究所 生命機能科学研究センター)
小坂田文隆 (名古屋大学大学院 創薬科学研究科)
1. 狂犬病ウイルスを用いた神経回路の可視化
神経系に感染するウイルスはニューロンからニューロンへと感染を広げる性質があるので神経回路の構造を標識する目的で利用することができる。このような神経回路トレーサーとしてのウイルスベクターの利用は1980年代に本格的に開始され、単純ヘルペスウイルス、偽狂犬病ウイルス、狂犬病ウイルスベクター等が開発された1。この中で狂犬病ウイルスは、i) 中枢神経系において完全に逆行性(シナプス後細胞からシナプス前細胞へと情報の流れと反対向き)に感染すること、ii) 比較的細胞毒性が低いこと、iii)通過しているだけの軸索には感染せず、シナプスを介してのみ感染が広がること (経シナプス性) という優れた性質を有し、多くの哺乳動物種で神経回路の標識に利用されている2。
2.G欠損型狂犬病ウイルスベクターと単シナプス標識
狂犬病ウイルスはマイナス一本鎖RNAをゲノムとするラブドウイルス科に属し、致死性の狂犬病の原因ウイルスである。狂犬病ウイルスのゲノムは約12 kbと小さく、核タンパク質N、マトリックスタンパク質M、RNA依存型RNAポリメラーゼL、ポリメラーゼ共因子リン酸化タンパク質P、及び膜糖たんぱく質Gの5種類のタンパク質をコードしている。ウイルスのコアはゲノムRNA、N、P、Lから構成され、Mに裏打ちされた脂質二重膜(宿主細胞に由来する)がコアを取り囲み、表面には膜糖タンパク質Gが配置されている (図1A)。1994年に機能的なウイルス粒子をプラスミドから再構成することが可能となり3、ウイルスゲノムの遺伝学的な改変への道が開かれた。続いて、1996年、弱毒株であるStreet Alabama Dufferin (SAD) B19株を用いてG遺伝子欠損型のゲノムを持つ狂犬病ウイルス (RV∆G) が初めて構成された4。RV∆Gはそのままでは感染可能な粒子とならないので、膜糖タンパク質Gをトランスジーンとして発現させた培養細胞を用いて再構成された(これをRV∆G+Gと表記する)。RV∆G+Gは機能的な膜糖たんぱく質Gを用いて哺乳動物の細胞に感染することはできるが、それ以上機能的なウイルス粒子を産生することはできないので、病原性が完全に失われている。
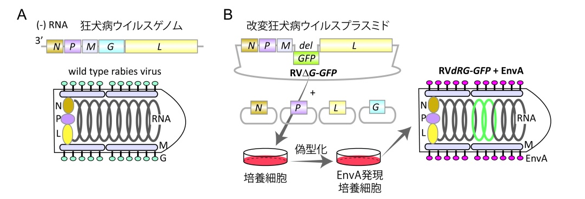
図1 狂犬病ウイルスの構造とG欠損型ウイルスベクター
単シナプス標識はRV∆Gベクターを用いて行われる。まず感染細胞を可視化する目的で、RV∆Gに蛍光タンパク質(GFPなど)を導入する。さらに、RV∆Gの初期感染を制御する目的で、トリ肉腫ウイルスのエンベロープタンパク質であるEnvAを用いて偽型化する (図1B)。こうして作成されたRV∆G-GFP+EnvAは哺乳類の細胞に受容体を持たないので一切感染することができないが、目的のニューロンにEnvAの受容体として機能するTVA受容体を発現させておくと特異的に感染させることができる。さらに同じニューロンに狂犬病ウイルスの糖タンパク質Gをトランスジーンとして発現させておくと、その細胞に限って機能的な粒子が再構成され、シナプス前細胞に感染する。しかし、シナプス前細胞はGを発現していないのでウイルスの感染はこれ以上広がることが無く、目的の細胞(これをstarter cellと呼ぶ)から一段階だけ上流のシナプス前細胞を特異的にGFPで標識することができる5。
単シナプス標識の利点として、i) starter
cellを遺伝学的に制御できるため、特定のタイプのニューロンを起点とした神経回路の構造を可視化できること、ii) ウイルスベクターが際限なく感染する多段階標識の系に比較して、直接性のシナプス接続だけを曖昧さなく可視化できること、iii) 病原性のないベクターを用いているので実験動物管理の点でも実験者のバイオセイフティ―の点でも安全性が高いこと、が挙げられる。
RV∆Gベクターはこれまでに異なる狂犬病ウイルス株から作製されているが、現在最も多く使用されているのがSADB19株由来である。ウイルス作製の詳細なプロトコールはNature Protocolsにて公開されている6。SADB19等固定株を用いた実験はP2/P2Aの実験施設を必要とする。また狂犬病ウイルスの接種実験やTVA受容体を発現する動物個体を作成する実験は一般的に文部科学大臣確認実験に該当すると考えられている他、適正な機関承認を要する。
3. Starter
cellsを遺伝学的に制御するいくつかの方法
ある脳領域に存在するニューロンの種類を規定する上で重要な4種類の指標が i) 遺伝子の発現パターン、ii) 形態 特に軸索投射パターン、iii) 発生プロファイル、iv) 活動パターンである。狂犬病ウイルスを用いた標識ではこれらの指標を遺伝学的に利用して特異的なstarter cellを作成することができる。
遺伝子の発現パターンを活用するためには標的遺伝子の発現制御下にCre組み換え酵素を発現するマウス系統を利用する (図2A)。このマウスの目的脳領域に対して脳定位固定装置を用いてCre依存的にTVA受容体と狂犬病ウイルスの膜糖タンパク質Gを発現させるようなアデノ随伴ウイルス (AAV) を導入する7,8。多くの場合にこれらのAAVには蛍光タンパク質による標識が導入してある (図2AのケースではTVAの発現に付随して赤色蛍光タンパク質mCherryが発現する)。AAVから発現したTVA受容体によって偽型化した狂犬病ウイルスベクターが感染し、Gによって径シナプス標識が開始される (図2B)。最終的に、starter cellはmCherryとGFPの二重陽性細胞、シナプス前ニューロンはGFPの単独陽性細胞として可視化される (図2C)。この手法は特定のタイプのニューロンを起点にした特異的な神経回路を可視化する目的でさまざまな脳領域において広く利用されている9。
軸索投射パターンに基づくstarter cellの作製には、軸索末端から効率よく取り込まれ逆行性に細胞体に感染してCreを発現させることのできるウイルスベクターが利用される10。たとえばイヌ科アデノウイルス(CAV2)、狂犬病ウイルスの膜糖タンパク質Gを用いて偽型化したレンチウイルス(加藤の稿参照)、retro-AAVなどがこの目的に利用できる。
、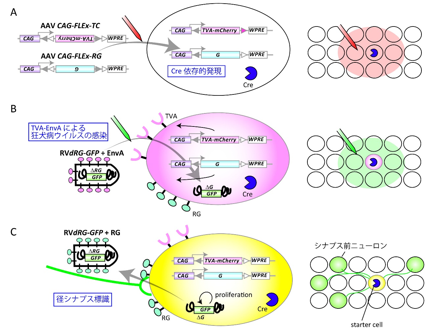
図2 狂犬病ウイルスを用いてCre依存的に径シナプス標識を行う手法
発生履歴を利用したstarter cell作製の一例として、標的ニューロンが分化したタイミングを用いる方法が挙げられる。子宮内電気穿孔法により発生過程の特定の時期にプラスミドを導入することによって、大脳の特定の層に位置するニューロンに特異的にアクセスできる。あるいは、分裂期の細胞に特異的に感染するレトロウイルスベクターを用いることで、生体脳において活発に新生を繰り返している海馬歯状回の顆粒細胞に特異的にアクセスできる。
最後に、活動パターンに基づくstarter cellの作製法として、初期応答遺伝子の一過的な活性化を利用して特定の刺激に応答したニューロンにアクセスする方法や、in vivoの一ニューロンにパッチクランプ法で電極を設置してその活動パターン (受容野など) を記録し、電気穿孔法によってプラスミドを導入することによって径シナプス標識のstarter cellに変換する方法などが報告されている。
参考文献
1 Vercelli A et al. Brain research bulletin 51, 11-28 (2000).
2 Ugolini G. Advances in virus research 79, 165-202 (2011).
3 Schnell MJ et al. Embo J 13, 4195-4203 (1994).
4 Mebatsion T et al. Cell 84, 941-951 (1996).
5 Wickersham IR et al. Neuron 53, 639-647 (2007).
6 Osakada F & Callaway EM. Nature protocols 8, 1583-1601 (2013).
7 Watabe-Uchida M et al. Neuron 74, 858-873 (2012).
8 Miyamichi K et al. Neuron 80, 1232-1245 (2013).
9 Callaway EM & Luo L. Journal of Neuroscience 35, 8979-8985 (2015).
10 Schwarz LA et al. Nature 524, 88-92 (2015).